塩素の同位体について考えよう
天然では、塩素原子は3517Clと3717Clの2種が存在する。そしてその存在比は3517Cl:3717Cl = 3:1である。
1: 塩素の原子量
2: Cl2の種類は何種類存在するか
3: 上の数種類Cl2の存在比
4: Cl2の分子量
上記の4つの量を求めましょう。
解答編
1: 塩素の原子量
原子量は原子の質量であり、原子質量単位(amu)/個の単位で表される量です。
そして各元素ごとに、それを構成する原子について原子量を求めるのですが、このクイズの塩素の同位体のように元素を構成する原子には2種類以上の種類があります。そこで原子量を求めるときは、存在比をもとに各原子の平均値を求める必要があります。
塩素は35Cl:37Cl = 3:1の個数比で存在しているので、塩素の原子量は次のような計算式で求めることになります。
各原子量は近似的に質量数とみなすことできるので、35Cl ≒ 35、37Cl ≒ 37となります。よって、下の式の計算結果から35.5が答えになります。
2: Cl2の種類は何種類存在するか
35Clと37Clの組み合わせを考えると下の図のように2×2 = 4通り考えられます。しかし左から2番目の35Clと37Clの組み合わせと左から3番目の37Clと35Clの組み合わせはひっくり返すと重なり、同じ分子です。よって答えは3種類となります。
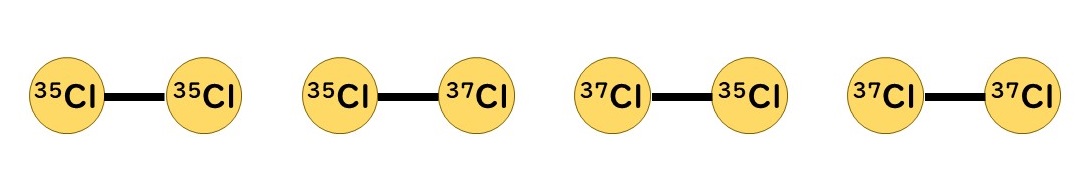
3: 上の数種類のCl2の存在比
35Clと37Clは陽子数、電子数、電子配置は同じなので、結合力もほぼ同じと考えることができます。
そのため、Cl2の存在比はもとのClの個数比を反映した単純な確率計算で求めることができます。
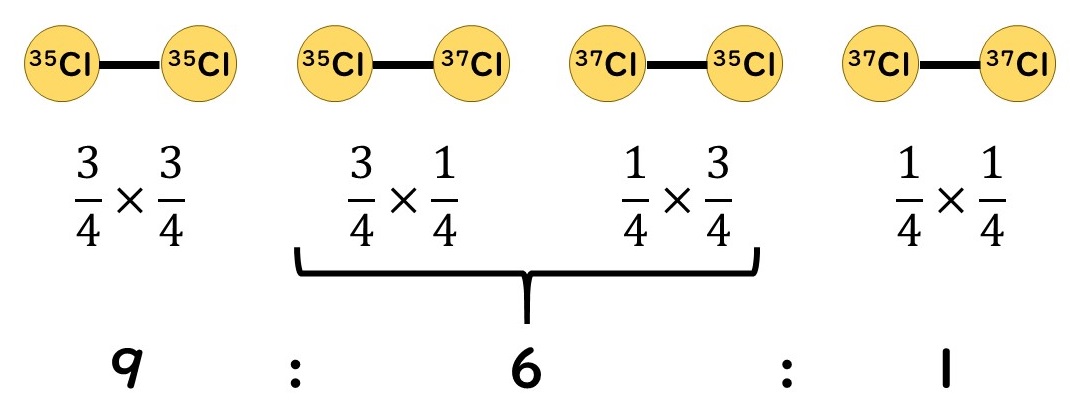
注意する点は左から2番目の組み合わせと左から3番目の組み合わせは同じ分子という点です。
4: Cl2の分子量
Cl2の分子量は、上の3種類の塩素分子の分子量と存在比から計算することができます。
35Clと35Clの分子は分子量70
35Clと37Clの分子は分子量72
37Clと37Clの分子は分子量74
よってCl2の分子量は下の計算式で71と求められます。